Ako pomenovať chemické zlúčeniny
Autor:
Laura McKinney
Dátum Stvorenia:
2 Apríl 2021
Dátum Aktualizácie:
26 V Júni 2024

Obsah
- stupňa
- Metóda 1 Nomenklatúra iónových zlúčenín
- Metóda 2 Nomenklatúra polyatomických zlúčenín
- Metóda 3 Nomenklatúra kovalentných zlúčenín
Úspech v oblasti chémie vyžaduje vedieť, ako pomenovať základné chemické zlúčeniny. Táto príručka vám poskytuje základné pravidlá týkajúce sa procesu pomenovávania chemických zlúčenín a toho, ako priradiť názvy zlúčeninám, ktoré sú pre vás neznáme.
stupňa
Metóda 1 Nomenklatúra iónových zlúčenín
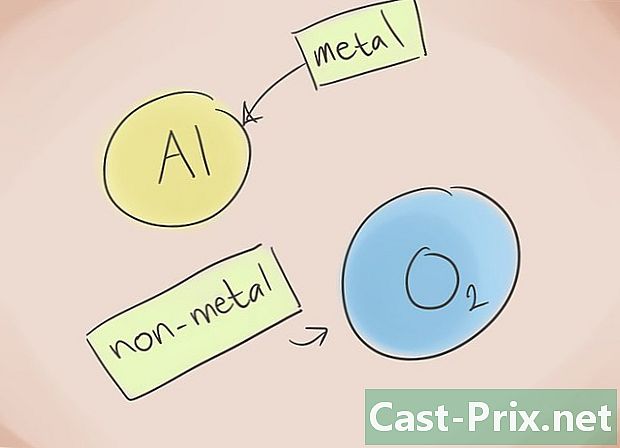
- Čo je to iónová zlúčenina? Iónové zlúčeniny pozostávajú z kovu a nekovu. Potom si pozrite periodickú tabuľku prvkov, aby ste vedeli, ktoré kategórie patria k prvkom prítomným v zlúčenine.
-

Vytvorte meno. Nič nie je ľahšie ako pomenovanie iónovej zlúčeniny z dvoch prvkov. Prvá časť názvu zlúčeniny skutočne zodpovedá názvu nekovového prvku s príponou „ure“, zatiaľ čo druhá časť zodpovedá názvu kovového prvku. Existujú výnimky: oxid, fosfid, nitrid, sulfid.- Príklad: Al2O3, al2 = Hliník; O3 = Kyslík. Názov zlúčeniny bude teda „oxid hlinitý“.
-
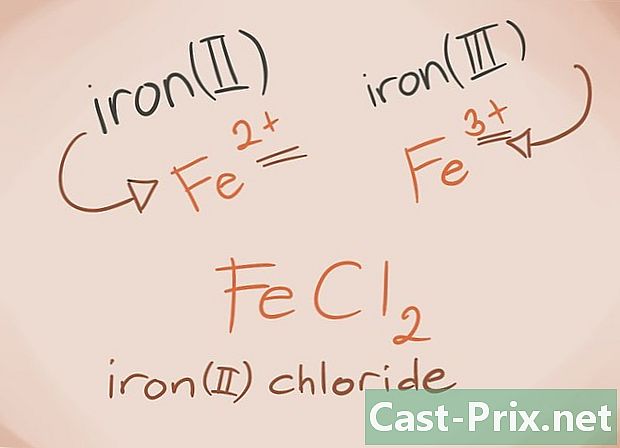
Poznajte prechodné kovy. Prechodné kovy sú tie, ktoré sa nachádzajú v blokoch D a F periodickej tabuľky. V mene zlúčeniny je poplatok za tieto kovy napísaný rímskymi číslicami. Dôvodom je, že prechodné kovy môžu niesť viac záťaže a vytvárať viac zlúčeniny.- Príklad: FeCl2 a FeCl3, Fe = železo; cl2 = -2 chlorid; cl3 = Chlorid -3. Ako názvy bude chlorid železitý (II) a chlorid železitý (III).
Metóda 2 Nomenklatúra polyatomických zlúčenín
-

Musíte pochopiť, čo je to polyatomická zlúčenina. Polyatomické zlúčeniny sú zlúčeniny tvorené skupinou navzájom spájaných datómov; celá skupina nesúca náboj je kladná alebo záporná. Na polyatomické zlúčeniny potom môžete uplatniť tri základné akcie:- K prvej časti zlúčeniny môžete pridať vodík. Slovo „vodík“ sa skutočne pridáva na začiatok názvu zlúčeniny. Tým sa zníži hodnota záporného náboja o jeden. Napríklad „uhličitanový“ CO3 sa stáva "hydrogenuhličitanom" HCO3.

- Zo zlúčeniny tiež môžete odstrániť kyslík. Zaťaženie sa nezmení, ale prípona "-ate" zlúčeniny sa zmení na "-ique". Napríklad transformácia: NIE3 v NO2 ideme z dusičnanu na dusičnan. "

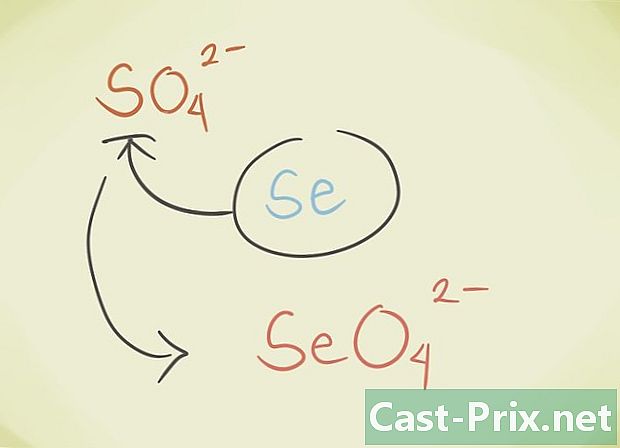
- Centrálny latóm zlúčeniny môžete nahradiť iným atómom patriacim do rovnakej periodickej skupiny. Napríklad síran sodný4 môže byť nahradený Selenate SeO4.
- K prvej časti zlúčeniny môžete pridať vodík. Slovo „vodík“ sa skutočne pridáva na začiatok názvu zlúčeniny. Tým sa zníži hodnota záporného náboja o jeden. Napríklad „uhličitanový“ CO3 sa stáva "hydrogenuhličitanom" HCO3.
-

Zapamätajte si najbežnejšie skupiny dionov. Skupiny uvedené nižšie sa používajú na vytvorenie väčšiny polyatomických zlúčenín. Po vzrastajúcom poradí ich záporného náboja máme:- hydroxidové ióny: OH
- dusičnanové ióny: NIE3
- Ióny uhličitanu vodíka: HCO3
- permanganátové ióny: MnO4
- uhličitanové ióny: CO3
- chromátové ióny: CrO4
- dichrómanové ióny: Cr2O7
- síranové ióny: SO4
- siričitanové ióny: SO3
- tiosíranové ióny: S203
- Fosfátové ióny: PO4
- amónne ióny: NH4
- Z vyššie uvedeného zoznamu vytvorte zložené názvy. Vytvorte priradenie názvu ku ktorejkoľvek z položiek súvisiacich so skupinou. Ak je prvok umiestnený pred iónovú skupinu, potom sa názov prvku jednoducho pridá na začiatok názvu zlúčeniny.
- Príklad: KMnO4, Musíte vedieť, že lev MnO4 zodpovedá manganistanu levu. K znamená draslík. Takže vaša zlúčenina sa bude nazývať permanganát draselný.
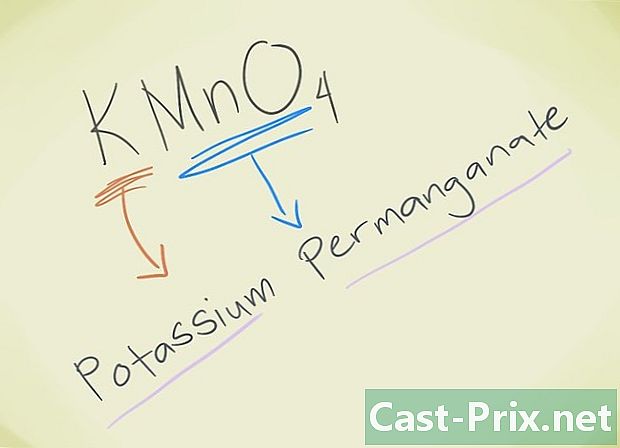
- Príklad: NaOH. Pravdepodobne ste tu pochopili, že je to OHOH. Na je sodík, takže zlúčenina sa bude nazývať hydroxid sodný.

- Príklad: KMnO4, Musíte vedieť, že lev MnO4 zodpovedá manganistanu levu. K znamená draslík. Takže vaša zlúčenina sa bude nazývať permanganát draselný.
Metóda 3 Nomenklatúra kovalentných zlúčenín
-
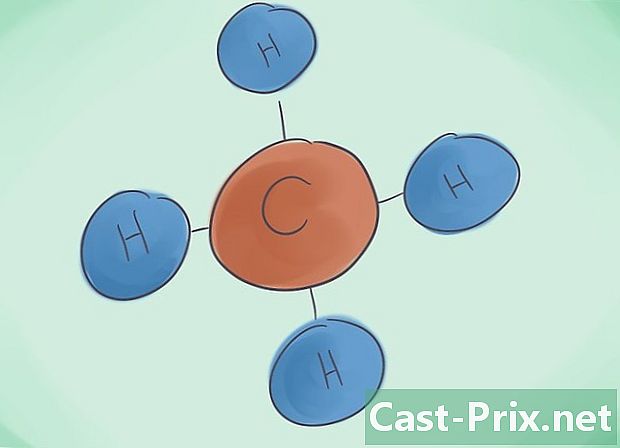
Čo je kovalentná zlúčenina? Kovalentné zlúčeniny sú výsledkom asociácie najmenej dvoch nekovových prvkov. Názov zlúčeniny je určený číselnými údajmi, ktoré ju tvoria. Grécka predpona vedľa tohto názvu označuje počet molekúl prítomných v zlúčenine. -
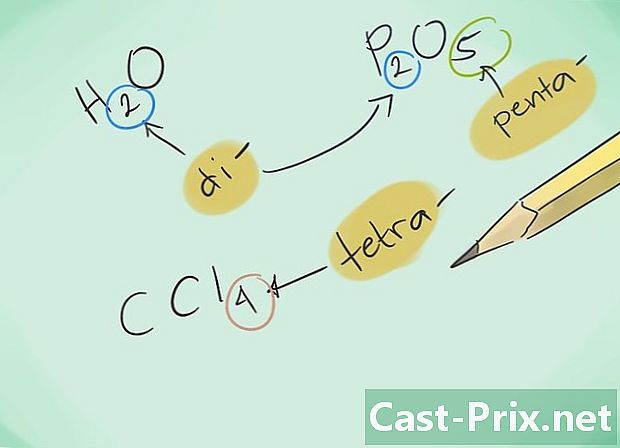
Oboznámte sa s predponami. Zapamätať si nasledujúce predpony pre zlúčeniny s 1 až 8 atómami:- 1 atóm - „Mono-“
- 2 atómy - „Di-“
- 3 atómy - „Tri-“
- 4 atómy - „Tetra-“
- 5 atómov - „Penta-“
- 6 atómov - „hexa“
- 7 atómov - „Hepta-“
- 8 atómov - „Octa-“
- Potom pomenujte zlúčeniny. Výslednú zlúčeninu pomenujte pomocou vhodných predpon. Predpony sa majú očkovať na každý z prvkov tvoriacich zlúčeninu s niekoľkými atómami.
- Príklad: CO sa vráti na oxid uhoľnatý, zatiaľ čo CO2 označí oxid uhličitý.
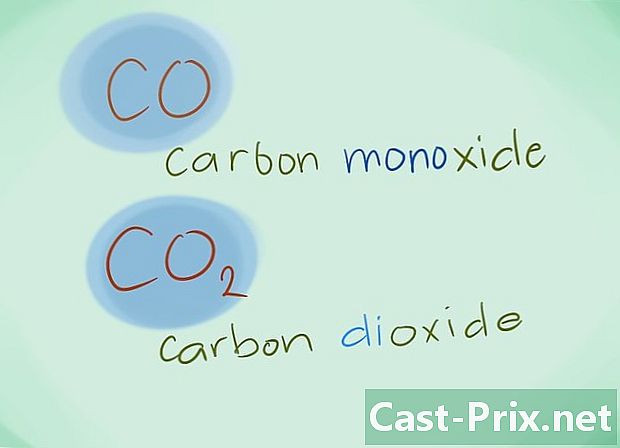
- Príklad: N2S3 by zodpovedal trisulfidu dusnatému.

- Vo väčšine prípadov možno predponu „mono“ vynechať; toto, viac ako akýkoľvek nedostatok predpony, naznačuje, že posledný by mal byť použitý. Táto predpona sa naďalej používa v prípade oxidu uhoľnatého vzhľadom na skutočnosť, že toto použitie siaha až do prvých trblietok chémie.
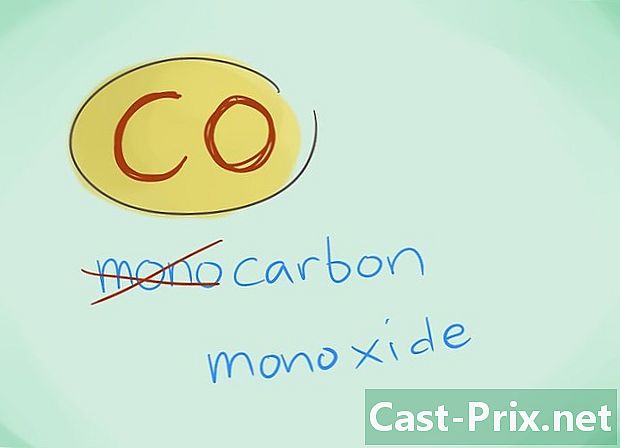
- Príklad: CO sa vráti na oxid uhoľnatý, zatiaľ čo CO2 označí oxid uhličitý.
- Máte samozrejme podozrenie, že na všetky tieto pravidlá sa vzťahuje niekoľko výnimiek; platí napríklad tento vzorec CaCl2Očakávate, že sa bude nazývať „chlorid vápenatý“, čo je NIE. Vaša zlúčenina si jednoducho ponechá názov chlorid vápenatý.
- Malo by sa tiež poznamenať, že toto všetko sa nevzťahuje na organickú chémiu.
- Podrobné pravidlá sú určené pre začiatočníkov z chémie a prírodných vied. Keď prechádzate štádiom pokročilej chémie, existujú veľmi odlišné pravidlá, napríklad pravidlá o premenlivej valencii.